Resumo de quimica: Modelos atômicos e partículas fundamentais - Thomson
O modelo seguinte ao modelo de Dalton que propunha que o átomo não era mais indivisível é o chamado modelo de Thomson. O segundo modelo ficou conhecido como modelo pudim de passas que já já a gente vai entender o porquê desse nome. O que motivou a dizer que o átomo não era mais indivisível foi a descoberta de uma partícula que era menor do que o átomo foi a descoberta do elétron.
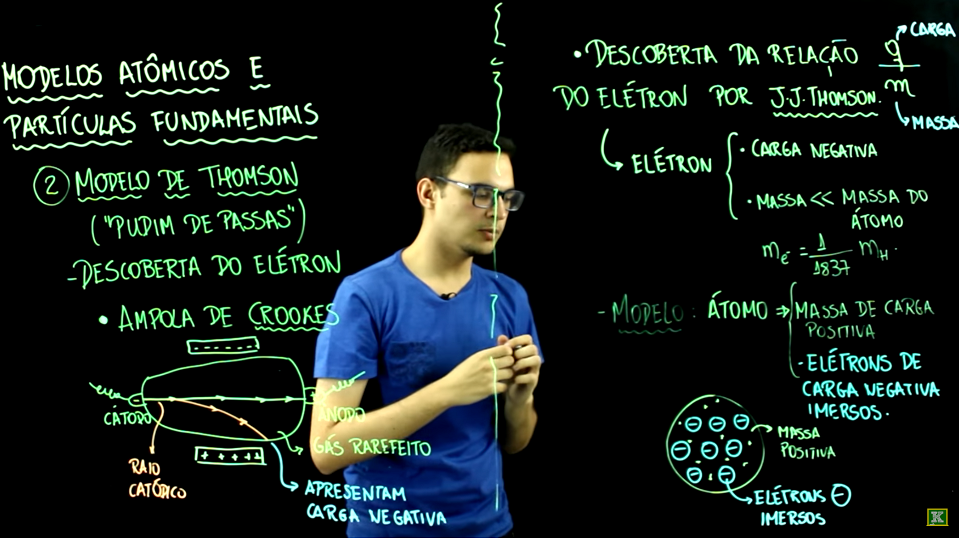
Como era o elétron? O que fez com que o elétron fosse descoberto? Basicamente foram dois fatos. O primeiro deles foi um experimento conhecido como ampola de Crookes. Basicamente, a ampola de Crookes tinha uma bola de vidro. Esta bola estava submetida à uma diferença de potencial, então desse lado do campo a gente tem um pólo negativo e desse lado aqui de campo a gente tem o pólo positivo. O pólo negativo é chamado de cátodo e o pólo positivo é chamado de ânodo. Existe uma diferença de potencial aqui, nos dois terminais, da ampola. Esta ampola estava preenchida por um gás a baixa pressão, gás rarefeito, que a gente escolheu para que este gás não interfira na trajetória dos raios produzidos a partir dessa diferença de potencial. Essa ampola é submetida a essa diferença de potencial gerava um raio que partia do cátodo para o ânodo. Como este raio parte sempre do cátodo para o ânodo, esse raio era chamado raio catódico. A pergunta do Crookes era qual a carga desse raio, será que esse raio é realmente eletricamente neutro ou será que ele tem carga positiva ou carga negativa? Para saber a resposta disso ele colocou aqui nas duas laterais da ampola um campo elétrico. Uma placa aqui em cima de carga negativa e aqui em baixo ele colocou uma placa de carga positiva. Aqui a gente vai ter que estabelecer um campo elétrico, então se esse raio tem carga positiva ele desviaria para cima, na parte da placa negativa e se ele tivesse carga negativa ele desviaria pra baixo, pra onde está a placa positiva e se tivesse carga neutra ele passaria que direto sem sofrer desvios.
O resultado disso foi que os raios catódicos gerados por essa diferença de potencial desviavam para placa positiva, o que significa que os raios catódicos apresentam carga negativa. Crookes a partir do seu experimento descobriu que os raios catódicos eram raios carregados que apresentavam carga negativa. Outro ponto que é importante para a proposta do modelo de Thomson foi a descoberta pelo próprio Thomson da relação entre a carga e a massa do elétron. Vamos chamar de q a carga e a massa de m. Este q/m, que é a carga do elétron e m é a massa do elétron, Thomson percebeu que os elétrons eram partículas de carga negativa e que possui massa muito menor do que a massa de um átomo seja qualquer átomo, até o átomo de hidrogênio que é o menor deles. Isto significou que o elétron possui carga negativa e massa muito menor do que a massa do átomo, aproximadamente mil oitocentos e trinta e sete vezes menor que a massa de um átomo de hidrogênio. O elétron era muito menor o que significa o que o elétron era uma partícula que era menor do que o átomo.
A proposta do modelo de Thomson era que o átomo era formado por uma massa de carga positiva com elétrons que possuíam carga negativa imersos na massa. Basicamente, a estrutura do modelo de Thomson era a seguinte eu continuo tendo uma esfera maciça assim como o modelo de Dalton só que essa espera não é mais indivisível, eu tenho aqui a massa, uma parte que tem carga positiva, e eu tenho os elétrons aqui imersos nessa massa, distribuídos uniformemente, com carga negativa. Então esse é o modelo de Thomson, a semelhança o pudim de passas é clara, a massa do pudim e do panetone tem carga positiva e os elétrons seriam as passas que tem carga negativa.






