(FUVEST - 2010 - 2 fase - Questo 5)Uma substncia p
(FUVEST - 2010 - 2 fase - Questão 5)
Uma substância pode apresentar solubilidades diferentes em solventes diversos. Assim, por exemplo, o ácido butanodioico é mais solúvel em água do que em éter. Ao misturar ácido butanodioico, éter e água, agitar a mistura e deixá-la em repouso por alguns minutos, separam-se duas fases, uma de éter e outra de água. Ambas contêm ácido butanodioico, em concentrações diferentes e que não mais se alteram, pois o sistema atingiu o equilíbrio.

Para determinar a constante desse equilíbrio, também chamada de coeficiente de partição, foram efetuados cinco experimentos. Em cada um, foi adicionado ácido butanodioico a uma mistura de 25 mL de água e 25 mL de éter. Após a agitação e separação das fases, as concentrações de ácido butanodioico, em cada fase, foram determinadas.
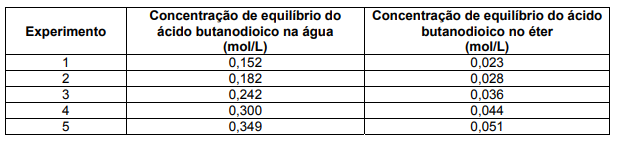
a) No quadriculado da folha de respostas, construa um gráfico da concentração de ácido butanodioico em éter versus a concentração de ácido butanodioico em água.
b) Calcule o valor do coeficiente de partição éter/água do ácido butanodioico.
c) Qual a massa, em gramas, de ácido butanodioico utilizada no experimento 5? Mostre os cálculos.
d) Em outro experimento, foram utilizadas duas diferentes amostras de ácido butanodioico. Uma delas continha, em suas moléculas, apenas o isótopo oxigênio-18, e a outra continha apenas oxigênio-16. A primeira (com oxigênio-18) foi adicionada à água, e a segunda (com oxigênio-16) foi adicionada ao éter. Após misturar as soluções, agitar a mistura e separar as fases, onde foi detectado o oxigênio-18? Explique.
Dado: massa molar do ácido butanodioico.........118 g/mol


