(UNESP - 2022 - 1 fase - DIA 2)Em um experimento d
(UNESP - 2022 - 1ª fase - DIA 2)
Em um experimento de calorimetria realizado no nível do mar, um estudante colocou 600 g de água a 10 ºC e 100 g de gelo a –40 ºC em um calorímetro ideal, onde já existiam 800 g de água a 5 ºC, em equilíbrio térmico com o calorímetro.
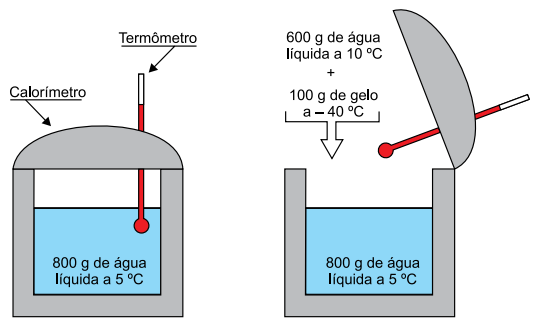
Sabendo que o calor específico da água líquida é 1 cal/(g·ºC), que o calor específico do gelo é 0,5 cal/(g·ºC) e que o calor latente de fusão do gelo é 80 cal/g, depois de atingido o novo equilíbrio térmico havia, dentro do calorímetro,
A
1500 g de água líquida a 10 ºC.
B
1450 g de água líquida e 50 g de gelo a 0 ºC.
C
1500 g de gelo a –5 ºC.
D
1500 g de água líquida a 0 ºC.
E
1500 g de gelo a 0 ºC.


