(IME 2022/2023 - 2 fase)Considere: Constante unive
(IME 2022/2023 - 2ª fase)
Considere:
- Constante universal dos gases ideais: \(R = 8,0\ J \cdot (mol \cdot K)^{-1} = 0,082 \ atm\cdot L \cdot (mol \cdot K)^{-1}\)
- Constante de Faraday = \(96500 \ C \cdot mol^{-1}\)
- \(K_{PS}(PbSO_{4}) = 1,3 \cdot 10^{-8}\) = 1,3×10−8
- Composicão molar do ar atmosférico: 79% de N2 e 21% de O2
- \(\sqrt{21,2} \simeq 4,6\)
- \(e^{1,1} \simeq 3\)
- \(e^{-0,17} \simeq 0,84\)
- \(286^{-1} \simeq 0,0035\)
- \(303^{-1} \simeq 0,0033\)
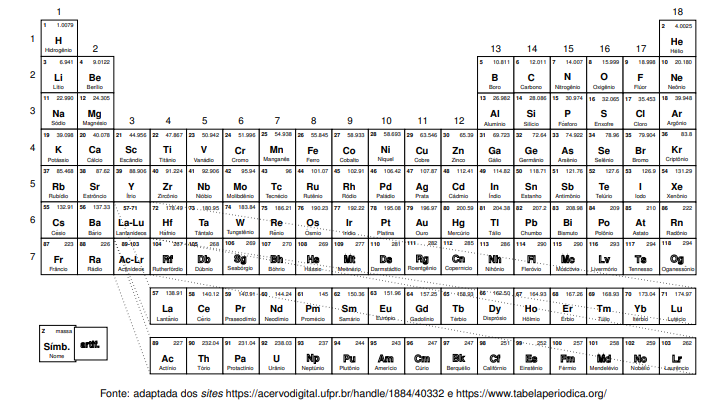
Tabela Periódica dos Elementos Químicos:
Seja a reação genérica balanceada:
\(A(g) + 2B (g) \rightleftharpoons C(s) + D(l)\)
Considere que: as solubilidades das especies químicas no líquido formado são desprezíveis; os gases se comportam idealmente; e as propriedades termodinâmicas a 1,0 atm e 30 ºC são as dadas abaixo.

Determine para essa reação:
a) a expressão da constante de equilíbrio com base nas concentrações \((K_{c})\);
b) o valor da constante de equilíbrio com base nas pressões parciais \((K_{p})\), a 30 ºC e 1 atm;
c) a variação de entalpia a 30 ºC e 1 atm, estabelecendo se a reação é exotérmica ou endotérmica;
d) o valor da constante de equilíbrio \(K_{p}\), a 13 ºC e 1 atm, com base na equação de Van’t Hoff:
\(ln\left ( \frac{K_{p,1}}{K_{p,2}} \right ) = \frac{-\Delta H^{\circ}}{R} \left ( \frac{1}{T_{1}} - \frac{1}{T_{2}} \right )\)


