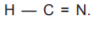(UEFS 2014 - Meio do ano)Os cidos so substncias qu
(UEFS 2014 - Meio do ano)
Os ácidos são substâncias químicas que se ionizam e liberam íons H+ em solução aquosa. A constante de ionização de um ácido, Ka, expressa a tendência do equilíbrio químico para a reação reversível de ionização de ácidos em solução aquosa.
Considerando-se as propriedades dos ácidos e a análise das informações da tabela, é correto concluir:
A reação de ionização do ácido fluorídrico produz mais íons em solução do que a do ácido nitroso.
A solução de HCN(aq) conduz corrente elétrica com mais eficiência do que a solução de HF(aq) de mesma concentração.
A substância química com maior tendência de liberar íons H+ em solução aquosa, dentre as apresentadas na tabela, é o HNO2.
O ácido fluorídrico é classificado como um hidrácido forte porque, em solução aquosa, a concentração de íons H3O+ é maior do que a de moléculas de HF
O HNO2 é representado pela fórmula estrutural
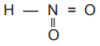
e o HCN por: